مهندس برتر
آموزش نیاز های ((اصلی و فرعی)) مهندس مکانیکمهندس برتر
آموزش نیاز های ((اصلی و فرعی)) مهندس مکانیکروزانهها
همه- سمینارهای اینترنتی سالیدروکس Solidworks Webinar
- آموزش تمام ابزارآلات مکانیکی
- آموزش فوق حرفه ای نرم افزار سالیدورکس SolidProfessor
پیوندها
- مهندس برتر(صفحه ی نخست)
- انجمن مهندسی مکانیک امریکا
- انجمن مهندسان مکانیک ایران
- آموزش انلاین ansys
- ترجمه ی آنلاین متن مترجم فوق پیشرفته فارسی به انگلیسی و انگلیسی به فارسی بچه های شریف
- آموزش Classpad کامل ترین مرجع آموزش استفاده از ماشین حساب کلاسپد
- دانلود پایان نامه فارسی دانلود فایل تمام متن پایان نامه های فارسی با محدودیت ۵ عدد در هفته (برای دسترسی باید عضو شوید)
- دانلود رایگان مقاله دانلود مقاله های علمی ISI توسط ایلرنیکا؛ در هر زمان و هر مکان مقالات انگلیسی خود را با استفاده از لینک و یا شناسه دیجیتال مقاله دانلود کنید!
- علم نت موتور جستجوی علمی با امکان جستجو در کلیه اسناد علمی فارسی در پایگاه های مختلف مانند مگیران، سیویلیکا، ایرانداک
- کنفرانس یاب جستجوی کنفرانس های داخلی و بین المللی
- فروشگاه و واژهنامه ابزارآلات ابزارمارت ویکی - شرح واژگان تخصصی مرتبط با ابزار آلات به زبان فارسی
- دانلود فایل های ۳بعدی سالیدورکس فایل های به اشتراک گذاشته شده در سایت رسمی Solidworks
- دانلود فایل های مخصوص پرینت ۳ بعدی
- آموزش درس کنترل - دانشگاه میشیگان آموزش های دانشگاه MICHIGAN برای درس Control به کمک Matlab&Simulink
- انتگرال گیری آنلاین
- تبدیل واحدها تبدیل تمام واحد های اندازه گیری به یکدیگر
- اصول نامه نگاری طریقه نوشتن نامه اداری و رسمی - نمونه نامه های اداری
دستهها
ابر برجسب
مکانیک خودرو اجزای ماشین متلب کتاب محاسبات عددی مکانیک ربات Numerical Analysis حل المسائل ارتعاشات matlab پایان نامه یاتاقان استاد مشاور استاد راهنما کلاس پد کلاسپد رضا میراب زادهبرگهها
- نرم افزار های رشته ی مکانیک
- English learning
- نانو تکنولوژی
- مطالب مفید و جالب
- کنکور ارشد
- جزوات رشته مکانیک
- نمونه سوالات رشته مکانیک
- دانستنی ها
- علم رباتیک
- زندگی نامه مشاهیر مهندسی مکانیک
- معرفی قطعات صنعتی
- هوافضا
- دانشگاه آزاد اسلامی واحد اهواز - رضا میراب زاده
- دانشکده فنی شهید چمران اهواز - رضا میراب زاده
- دانشکده فنی شهدای اهواز - رضا میراب زاده
- دانشگاه علمی و کاربردی اهواز - رضا میراب زاده
جدیدترین یادداشتها
همه- آموزش کولیس
- رفع مشکل ارور { PAGE \* MERGEFORMAT } در وورد
- آموزش نرم افزار Mimics برای مدل سازی تصاویر سه بعدی پزشکی
- 99 تجربه برای دانشجویان دوره کارشناسی (لیسانس) نوشته مسعود گوهری منش
- نقش استاد راهنما، مشاور و داور در فرایند تدوین پایان نامه
- دانلود آموزش مقدماتی کد نویسی در ماشین حساب Classpad
- دانلود جامع ترین کتاب آموزش پنوماتیک فارسی زبان
- Team Work...
- ترسیم دیاگرام بود و نایکویسست بکمک کلاس پد
- اطلاعیه- دانلود کتاب ها
بایگانی
- مرداد 1398 1
- آذر 1397 1
- تیر 1397 1
- آذر 1396 1
- اردیبهشت 1395 1
- بهمن 1394 3
- دی 1394 2
- آبان 1394 1
- مهر 1394 3
- مرداد 1394 11
- تیر 1394 7
- خرداد 1394 18
- اردیبهشت 1394 6
- فروردین 1394 5
- اسفند 1393 6
- بهمن 1393 1
- دی 1393 4
- آذر 1393 25
- تیر 1393 1
- مرداد 1391 1
- خرداد 1391 1
- اسفند 1390 1
- بهمن 1390 1
- آذر 1390 2
- آبان 1390 3
- مهر 1390 6
- شهریور 1390 7
- مرداد 1390 12
- تیر 1390 6
- خرداد 1390 4
- اردیبهشت 1390 19
- فروردین 1390 14
- اسفند 1389 16
- بهمن 1389 16
- دی 1389 4
- آذر 1389 19
- آبان 1389 16
- مهر 1389 30
- شهریور 1389 45
- مرداد 1389 27
- تیر 1389 37
- خرداد 1389 22
- اردیبهشت 1389 21
- فروردین 1389 18
- اسفند 1388 23
- بهمن 1388 2
تقویم
مرداد 1398| ش | ی | د | س | چ | پ | ج |
| 1 | 2 | 3 | 4 | |||
| 5 | 6 | 7 | 8 | 9 | 10 | 11 |
| 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 |
| 26 | 27 | 28 | 29 | 30 | 31 |
جستجو در این وبلاگ
قانون اول ترمودینامیک

قانون اول ترمودینامیک که به عنوان قانون بقای کار و انرژی نیز شناخته میشود، میگوید که حالت تعادل ماکروسکوپی یک سیستم با کمیتی به نام انرژی درونی (U) بیان میشود.
انرژی درونی دارای خاصیتی است که برای یک سیستم منزوی (ایزوله) داریم:
اگر به سیستم اجازهٔ برهمکنش با محیط داده شود، سیستم از حالت ماکروسکوپی اولیهٔ خود به حالت ماکروسکوپی دیگری منتقل میشود که تغییر انرژی درونی را برای این تحول (فرآیند) میتوان به شکل زیر نشان داد:
که در این فرمول W، کار ماکروسکوپی انجام شده توسط سیستم در برابر نیروی خارجی و Q مقدار گرمای جذب شده توسط سیستم در طی این فرآیند است.
نمادگذاری
شیمی و فیزیک
چون در شیمی و فیزیک سیستم مورد توجهاست، گرما و کاری که به سیتم داده میشود مورد نظر ماست و انرژی درونی را Q+W در نظر میگیریم. (سیستم را بسته، در حالت سکون و در غیاب میدانها در نظر میگیریم)
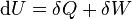
که در آن- dU یک افزایش بیاندازه کوچک در انرژی درونی سیستم است.,
- δQ یک مقدار بیاندازه کوچک از گرما که به سیستم افزوده میشود,
- δW یک کار بیاندازه کوچک که بر روی سیستم انجام میشود و
- δ نماد دیفرانسیل است.
در واقع تعریف قانون اول چنین است : اگر به سیستمی گرما داده شود و یا از آن گرما گرفته شود، انرژی درونی سیستم تغییر خواهد نمود که حاصل آن کار انجامشده توسط سیستم و یا کار مورد نیاز سیستم برای تغییر انرژی درونی خواهد بود .


























